|

por Rosemary Frei
26 Enero
2022
del Sitio Web
RosemaryFrei
traducción de
SOTT
26 Enero
2022
del
Sitio Web
SOTT
Versión original en ingles
Versión
en italiano
|
Tras obtener un master en
biología molecular en la Facultad de Medicina de la
Universidad de Calgary, Rosemary Frei se convirtió en
escritora independiente.
Durante los siguientes 22
años fue escritora y periodista médica.
A principios de 2016
volvió a dedicarse a tiempo completo al activismo
independiente y al periodismo de investigación.
Su Sitio Web es
RosemaryFrei.ca. |

El Paxlovid de Pfizer se está extendiendo por todo el mundo.
Pero en cierto modo es
aún más experimental que la
inyección antiCovid de la compañía
farmacéutica.
El Ministerio de Sanidad
de Canadá, al igual que
la FDA de EE.UU., aliada de la industria
farmacéutica desde hace décadas, admite que,
"no muchas personas
han tomado Paxlovid. Pueden producirse efectos secundarios
graves e inesperados".
Los gigantescos convoyes
de camiones se dirigen hacia Ottawa, acompañados de una gran
cantidad de simpatizantes y de la cobertura de los medios de
comunicación.
Sin embargo, al mismo tiempo, el Paxlovid de Pfizer está empezando a
distribuirse de forma relativamente silenciosa por Norteamérica,
Europa, Reino Unido y otros países.
Se trata de un
conjunto de píldoras para la Covid, y es la segunda parte de un
golpe de efecto que comenzó con la
inyección de ARNm antiCovid
de la empresa.
Juntos, están
impulsando a Pfizer a niveles vertiginosos de beneficios y
capitalización bursátil...
Sin embargo, es poco probable que estas píldoras produzcan "pax"
(palabra latina para paz).
El Paxlovid se ha
probado en muy pocas personas hasta ahora. No se ha estudiado en
absoluto en personas vacunadas o que hayan tenido Covid.
Las píldoras
interactúan negativamente con
muchos medicamentos muy utilizados. Además, por supuesto,
los estudios están siendo manipulados para producir resultados
aparentemente buenos.
He oído que, entre bastidores,
algunos empleados de las agencias reguladoras están hartos de ceder
a la intensa presión de los políticos, los funcionarios de salud
pública y las grandes farmacéuticas.
No quieren que los ciudadanos
tomen este conjunto de píldoras extremadamente mal estudiadas y
potencialmente muy peligrosas.
Cada dosis de Paxlovid consta de,
-
un comprimido de
ritonavir,
un antiguo
medicamento anti-VIH reutilizado
-
dos de un nuevo fármaco
llamado nirmatrelvir...
Ambos medicamentos
son inhibidores de
la proteasa.
La combinación nirmatrelvir/ritonavir fue autorizada por la
Administración de Alimentos y Medicamentos de EE.UU. en virtud de
una autorización de uso de
emergencia (EUA) el
22 de diciembre de 2021, y por el Ministerio de Salud de Canadá
el
17 de enero de 2022.
Además, se está aprobando rápidamente en otros países:
por
ejemplo, recibió el visto bueno en
Israel el
26 de diciembre de 2021, en
Corea del Sur el
27 de diciembre de 2021, en el
Reino Unido el
31 de diciembre de 2021 y en
Francia el
21 de enero de 2022.
Está permitida en
jóvenes a partir de 12 años y en adultos en Estados Unidos, Israel y
Corea del Sur.
En otros países,
como el
Reino Unido y
Canadá, está autorizada para mayores de 18 años.
Observe que la autorización no es
una aprobación; es una evaluación muy rápida seguida del
visto bueno para que decenas de millones de personas lo tomen,
porque supuestamente estamos en una 'crisis' de salud pública sin
precedentes, similar a una guerra.
Además, una prueba en una placa de Petri realizada por científicos
de Pfizer demostró que puede tener algún efecto sobre ómicron (véase
el primer párrafo de la página 36 de la hoja de especificaciones
canadiense del
22 de enero, conocido como 'monografía del producto') sobre el
mismo.
Basándose en estas escasas pruebas,
los
principales medios están informando ampliamente de que,
"se
espera que las píldoras sean eficaces contra la ómicron".
Las píldoras de nirmatrelvir/ritonavir están siendo autorizadas para
su uso por parte de las personas que dan positivo en la prueba de
Covid, tienen síntomas leves o moderados y se considera que están,
"en alto riesgo
de progresión a Covid-19 grave"...
¿Pero cómo define Pfizer el alto riesgo?
Tener 60 años o más, o tener sobrepeso, o tener la presión arterial
alta, o una serie de otras cosas, incluyendo tener,
"otras
condiciones o factores (es decir, la raza o el origen étnico)
que pueden colocar a los pacientes en alto riesgo de progresión"
(véase la página 8 de la hoja de especificaciones canadiense del
22 de enero).
Se trata de una
definición extremadamente amplia.
Otro hecho alarmante es que las
decisiones estadounidenses y canadienses de autorizar nirmatrelvir/ritonavir
se basaron únicamente en los análisis provisionales de un estudio en
curso.
Este ensayo
comenzó el 25 de agosto de 2021 y está previsto que finalice
aproximadamente el 24 de abril de 2022.
En total, sólo unas 1.000 personas
habían sido barajadas para recibir nirmatrelvir/ritonavir en el
momento en que las autoridades estadounidenses y canadienses le
dieron el visto bueno.
Es muy difícil averiguar cuáles son las cifras concretas:
tanto el
comunicado de prensa de Pfizer del
5 de noviembre de 2021, que describe el análisis provisional
examinado por la FDA, como la
monografía del producto canadiense del 17 de enero de 2022 (que
tiene un análisis provisional de una fecha ligeramente posterior)
tienen un rango de cifras, así como varios tipos de análisis de
datos.
Además, sólo el 13% de ese pequeño
número eran personas de 65 años o más, y sólo el 3% tenían 75 años o
más (véase la sección 1.2, titulada "Geriatría", en la
página 4 de la
monografía del producto canadiense de Paxlovid de 17 de enero de
2022).
Además, incluso esos resultados
provisionales se manipularon al máximo en la redacción del estudio
(más sobre esto a continuación), que en el caso de los Estados
Unidos fue simplemente un
comunicado de prensa de Pfizer de 5 de noviembre de 2021.

Y Pfizer ni siquiera hizo públicos los
datos originales que suministró al Ministerio de Salud de Canadá,
por lo que puedo determinar.
Además, el
comunicado de prensa de la compañía del
17 de enero de 2022 en el que se anunciaba la autorización en
Canadá tenía muy pocos detalles.
Todo era muy
predecible
Esto es obvio por el hecho de que más de un mes antes de la
autorización de la FDA (el
18 de noviembre de 2021) el gobierno de EE.UU. firmó un acuerdo
de 5.300 millones de dólares para 10 millones de ciclos de
nirmatrelvir/ritonavir (es decir, 530 dólares por ciclo),
a la espera de la autorización de
la FDA.
Lo mismo ocurre en Canadá:
el
3 de diciembre de 2021, el gobierno canadiense anunció su
compromiso de comprar a Pfizer un millón de ciclos iniciales de
nirmatrelvir/ritonavir, a la espera de la autorización del
Ministerio de Salud de Canadá.
Esto supone unos
690 millones de dólares canadienses si se hacen las cuentas sobre la
base de 530 dólares estadounidenses por ciclo (un "ciclo" significa
el número total de dosis necesarias para completar un régimen de
tratamiento).
El mismo anuncio decía que el gobierno canadiense
también había firmado un acuerdo
con Merck para comprar 500.000 ciclos de la
píldora antiCovid de Merck, el molnupiravir, con opciones para
comprar 500.000 ciclos más, también pendiente de la autorización del
Ministerio de Salud de Canadá.
El molnupiravir fue
autorizado por la FDA de EE.UU. poco después, el
23 de diciembre de 2021, a pesar de las
importantes preocupaciones.
Entre ellas,
su
escasa eficacia,
su elevada toxicidad y la posibilidad de que las mujeres que lo
tomen durante el embarazo den a luz a niños con defectos
congénitos.
La FDA autorizó
a Merck a venderlo para personas de 18 años o más con Covid leve
a moderada que den positivo y tengan un "alto riesgo" de
desarrollar Covid grave.
El Ministerio
de Salud de Canadá aún no le ha dado el visto bueno.
Y los
medios informan de que otros países también se están
arrepintiendo...
Hay más.
Por ejemplo, el nirmatrelvir/ritonavir
no ha sido probado en absoluto en personas que no han sido
vacunadas y no han tenido Covid.
A pesar
de ello, se encuentran entre las personas que las autoridades
quieren que sean las primeras en recibirlo.
Tampoco se ha probado en
absoluto en mujeres embarazadas o en periodo de lactancia.
Pfizer afirma en la página 12 de la
monografía del producto que Paxlovid,
"no debe utilizarse en
embarazadas a menos que los beneficios potenciales superen los
riesgos potenciales para el feto".
Pero no hay ninguna advertencia de
este tipo para el uso de nirmatrelvir/ritonavir por parte de las
mujeres en periodo de lactancia.
Como he señalado antes en este artículo, cada dosis de Paxlovid
consta de dos comprimidos de nirmaltrelvir y un comprimido de
ritonavir.
Cada juego de tres
comprimidos debe tomarse dos veces al día durante cinco días,
empezando en los cinco días siguientes al inicio de los síntomas.
El
ritonavir se utiliza desde 1996 en personas que dan positivo en
la prueba del VIH.
Es ampliamente conocido por causar
afecciones graves y potencialmente mortales, como pancreatitis,
problemas del ritmo cardíaco, problemas hepáticos, erupciones
cutáneas graves y reacciones alérgicas.
Sin embargo, el nirmatrelvir/ritonavir no se ha estudiado en
personas con insuficiencia hepática.
Y ni Pfizer ni las
autoridades gubernamentales advierten de que el nirmatrelvir/ritonavir
no debe ser tomado, por ejemplo, por personas con riesgo de
desarrollar una función hepática anormal (incluidas las que han
tenido hepatitis B, hepatitis C o resultados elevados en las pruebas
de función hepática).
En su lugar, están poniendo en
primera línea a los ancianos y a los que viven en la pobreza o están
desfavorecidos por otros motivos.
Un
artículo de CBC News del 25 de enero informa de que el
subdirector de salud pública de Canadá, Howard Njoo, recomienda que,
"las personas
inmunodeprimidas, de 80 años o más, o [aquellas] que no tengan
acceso a la atención sanitaria por motivos geográficos o
socioeconómicos[,] sean los primeros en recibirlas,
independientemente de su estado
de vacunación".
Quebec es uno de los primeros
lugares preparados para empezar a utilizarla en estas
personas vulnerables.
Para marzo esperan
recibir suficientes pastillas para tratar a más de 25.000 personas.
Eso incluye a los
que tienen,
"enfermedades
graves que no pueden ser vacunados".
Después de eso,
abrirán la lista a otros.
Por lo tanto, parece que los
políticos, los funcionarios del gobierno y Pfizer están alimentando
la demanda utilizando el mismo libro de jugadas que hicieron con las
vacunas.
Sólo están poniendo a disposición un número relativamente pequeño de
píldoras al principio. Y los principales medios de
comunicación están ayudando a darle bombo.
Por ejemplo, un
solo informe de la CBC realizado por la periodista de Montreal
Verity Stevenson el
18 de enero lo calificó como un fármaco "codiciado"
que ha sido,
"alabado
por su potencial para reducir las hospitalizaciones por el virus"
a través de la información de Pfizer de que "Paxlovid redujo el
riesgo de hospitalización o muerte en un impresionante 89% en
comparación con un placebo".
Y aquí hay otro
ejemplo de la muy positiva cobertura general; está en el
Toronto Star de hoy.
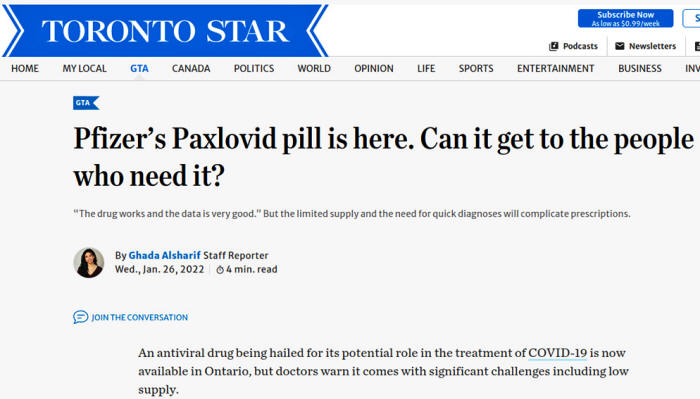
Captura de pantalla
del Toronto Star
Un artículo del
National Post del
25 de enero de 2022 es en cierto modo una excepción:
el autor,
Tom Blackwell, señala el problema de que el Paxlovid
interfiere con los efectos de otros medicamentos (más sobre esto
a continuación).
Sin embargo, no
menciona la mayoría de los demás inconvenientes importantes de las
píldoras.
Sin embargo, incluso el gobierno federal canadiense admite, en su
página web para el público en general sobre la píldora, que,
"no
muchas personas han tomado Paxlovid. Pueden producirse efectos
secundarios graves e inesperados".
"El Paxlovid
todavía se está estudiando, por lo que es posible que no se
conozcan todos los efectos secundarios en este momento".

Y más abajo en esa
misma página dice que la gente debe informar de cualquier sospecha
de efectos secundarios directamente al Ministerio de Salud de
Canadá.
Desgraciadamente, sin embargo, sabemos por los escasos informes de
efectos graves y muertes de, por ejemplo, las inyecciones antiCovid,
que es muy poco probable que los
federales cuenten fielmente y muestren públicamente todos esos
informes.
Por su parte, la
FDA pidió a Pfizer
que le informara de,
"los efectos
adversos graves y todos los errores de medicación asociados al
uso de Paxlovid", como parte de la EUA.
También estipuló
que los centros de salud y los proveedores de atención sanitaria que
reciban Paxlovid harán un seguimiento y comunicarán los
acontecimientos adversos graves y los errores de medicación.
Sin embargo,
es muy poco probable que esto dé
lugar a una información pública completa y honesta.
La FDA también ha pedido a la empresa que le proporcione más
resultados del ensayo relacionados con la seguridad y la eficacia
hasta que el estudio concluya en abril.
Así que ni siquiera intentan fingir
que se ha demostrado que es seguro y eficaz.
Después de todo, estamos en la
época del farmacoceno de la historia de nuestro planeta.
Aquí hay tres banderas rojas más entre las muchas que rodean al
Paxlovid:
-
La FDA de EE.UU. omitió el
importante paso de obtener la opinión de un panel asesor
antes de dar una autorización de uso de emergencia al
Paxlovid.
Ese panel
se llama Comité Asesor de Medicamentos Antimicrobianos.
Los
miembros del panel examinan los datos de las compañías
farmacéuticas sobre los medicamentos que las empresas
quieren aprobar.
Las reuniones del panel son públicas y a
ellas asisten los medios de comunicación y otras personas.
En cambio, en el caso del molnupiravir se convocó, a finales
de noviembre de 2021 [los miembros
votaron a favor, 13 a 10, y el 23 de diciembre de 2021,
la FDA lo autorizó].
Lo descubrí cuando me topé con un artículo de
SonsOfLibertyMedia.com del
6 de enero de 2022 sobre el Paxlovid.
El artículo
describe, entre otras muchas informaciones, este otro
artículo del
22 de diciembre de 2021 de Bloomberg Law sobre
la controversia causada por la FDA al saltarse este
importante paso.
Las reuniones del panel suelen ser un mero trámite, pero sin
embargo saltárselo es muy inusual.
-
Además de ser un inhibidor de
la proteasa, el ritonavir reduce la actividad de una enzima
muy importante llamada
CYP3A4.
El CYP3A4 se produce en el
hígado. Allí, es fundamental para metabolizar (es decir,
descomponer) un gran número de fármacos y toxinas; esto es
necesario antes de que los fármacos y las toxinas puedan ser
eliminados del organismo.
Dado que el
ritonavir (y, por extensión, el Paxlovid) reduce la
actividad del CYP3A4, esto significa que ese gran número de
fármacos y toxinas
permanecerán más tiempo en el organismo.
El
sitio web del gobierno federal canadiense sobre el Paxlovid
admite que "muchos
medicamentos interactúan con el Paxlovid.
Tomar Paxlovid con estos
medicamentos puede provocar efectos secundarios graves o
potencialmente mortales".
En total, hay más de 100
medicamentos que, según Pfizer, no deben tomarse con
Paxlovid.
Entre ellos
se encuentran algunos muy utilizados, como la lidocaína, la
warfarina, el fenobarbital, la eritromicina, la hierba de
San Juan, el fentanilo, la metadona, el midazolam y la
prednisona.
-
Los resultados del estudio que
aparecen en el comunicado de prensa estadounidense del
5 de noviembre de 2021 de Pfizer se basan en análisis
estadísticos "por intención de tratar".
Estos no son en absoluto
rigurosos.
Si busca lo
que significa "intención de tratar", verá que se basa en
asumir que los sujetos del estudio recibieron el
tratamiento, lo hayan hecho o no.
Muchos
artículos sobre este enfoque lo consideran sólido.
Pero
objetivamente no lo es en absoluto (empecé a fijarme en los
análisis por intención de tratar en los estudios de
investigación médica hace al menos 20 años; eran, y siguen
siendo, por lo que sé, una forma popular de evitar la
información honesta sobre los efectos y la eficacia de los
medicamentos que se prueban).
Y para que quede claro, el estudio de Pfizer no se detuvo
ahí: sus análisis con intención de tratar utilizan un
enfoque "modificado".
Específicamente incluyen, por ejemplo, a las personas,
"que al
inicio del estudio no recibían ni se esperaba que
recibieran el tratamiento anti-Covid-19 con el mAb
[anticuerpo monoclonal]".
No se pueden inventar estas cosas.
Espero sinceramente que los
empleados que, entre bastidores, se oponen a la presión para que se
administre Paxlovid a muchas personas, se impongan.
|