|
di Rosemary Frei 26 Gennaio 2022 del Sito Web RosemaryFrei traduzione di Nicoletta Marino
Il Paxlovid di Pfizer si sta diffondendo in tutto il mondo.
Ma in un certo senso è ancora più sperimentale dell'iniezione anti-Covid dell'azienda farmaceutica .
Health Canada, come la US FDA, alleata dell'industria farmaceutica per decenni, ammette che:
I giganteschi convogli di camion si dirigono verso Ottawa, accompagnati da un gran numero di sostenitori e dalla copertura mediatica.
Allo stesso tempo, tuttavia, Paxlovid di Pfizer, sta iniziando a essere spedita in modo relativamente silenzioso in Nord America, Europa, Regno Unito e altri paesi.
È un set di pillole per il Covid, ed è la seconda parte di un colpo di stato iniziato con l'iniezione di mRNA anti-Covid da parte dell'azienda.
Tuttavia, è improbabile che queste pillole producano "pax" (in latino pace).
Finora Paxlovid è stato testato in pochissime persone. Non è stato affatto studiato nelle persone che sono state vaccinate o che hanno avuto il Covid.
Le pillole interagiscono negativamente con molti farmaci ampiamente utilizzati. Inoltre, naturalmente, gli studi vengono manipolati per produrre risultati apparentemente buoni.
Ho sentito che, dietro le quinte, alcuni dipendenti delle agenzie di regolamentazione sono stufi di cedere alle intense pressioni di politici, funzionari della sanità pubblica e Big Pharma.
Non vogliono che i cittadini prendano questo set di pillole estremamente poco studiato e potenzialmente molto pericoloso.
Ogni dose di Paxlovid è composta da:
Entrambi i farmaci sono inibitori della proteasi.
Nirmatrelvir/ritonavir è stato autorizzato dalla Food and Drug Administration statunitense in base a un'autorizzazione all'uso di emergenza (EUA) il 22 dicembre 2021 e da Health Canada il 17 gennaio 2022.
Inoltre, è stato rapidamente approvato in altri paesi:
È consentito nei giovani dai 12 anni e negli adulti negli Stati Uniti, Israele e Corea del Sud.
In altri paesi, come Regno Unito e Canada, è autorizzato per i maggiori di 18 anni.
Si noti che l'autorizzazione non è un'approvazione; è uno screening molto rapido seguito dal via libera per decine di milioni di persone, perché presumibilmente siamo in una "crisi" della salute pubblica senza precedenti, simile a una guerra .
Inoltre, un test con piastre di Petri condotto da scienziati Pfizer ha mostrato che potrebbe avere qualche effetto sull'omicron (vedi primo paragrafo a pagina 36 della scheda tecnica canadese del 22 gennaio), noto come "monografia del prodotto").
Sulla base di queste scarse prove, i media tradizionali stanno ampiamente riportando che si tratta di
Le pillole di Nirmatrelvir/ritonavir sono autorizzate per l'uso da parte di persone che risultano positive al Covid, hanno sintomi lievi o moderati e sono considerate,
Ma come definisce Pfizer un rischio elevato?
Avere 60 anni o più, o essere in sovrappeso, o avere la pressione alta, o una serie di altre cose, incluso avere,
Questa è una definizione estremamente ampia.
Un altro fatto allarmante è che le decisioni statunitensi e canadesi di concedere in licenza nirmatrelvir/ritonavir si basavano esclusivamente su analisi provvisorie di uno studio in corso.
In totale, solo circa 1.000 persone erano state prese in considerazione per ricevere nirmatrelvir/ritonavir nel momento in cui le autorità statunitensi e canadesi hanno dato il via libera.
È molto difficile scoprire quali siano le cifre specifiche:
Inoltre, solo il 13% di quel piccolo numero era costituito da persone di età pari o superiore a 65 anni e solo il 3% aveva almeno 75 anni di età (vedere la sezione 1.2, intitolata "Geriatria", a pagina 4 della monografia canadese del prodotto di Paxlovid da 17 gennaio 2022).
Inoltre, anche quei risultati provvisori sono stati pesantemente manipolati nella stesura dello studio (ne parleremo più avanti), che nel caso degli Stati Uniti era semplicemente un comunicato stampa Pfizer del 5 novembre 2021.
E la Pfizer non ha nemmeno rilasciato i dati originali forniti a Health Canada, per quanto ne so.
Inoltre, il comunicato stampa della società del 17 gennaio 2022 che annunciava l'autorizzazione canadese conteneva pochissimi dettagli.
Era tutto molto prevedibile
Questo è evidente dal fatto che più di un mese prima dell'approvazione della FDA (il 18 novembre 2021) il governo degli Stati Uniti ha firmato un accordo da 5,3 miliardi di dollari per 10 milioni di cicli di nirmatrelvir/ritonavir (cioè, 530 dollari per ciclo ), in attesa dell'autorizzazione della FDA.
Lo stesso vale in Canada:
Lo stesso annuncio affermava che il governo canadese aveva anche firmato un accordo con Merck per l'acquisto di 500.000 cicli della pillola anti-Covid di Merck, molnupiravir, con opzioni per l'acquisto di ulteriori 500.000 cicli, anche in attesa dell'autorizzazione di Health Canada.
Molnupiravir è stato autorizzato dalla FDA statunitense poco dopo, il 23 dicembre 2021, nonostante le preoccupazioni significative.
Tra queste:
Health Canada non ha ancora dato il via libera.
E i media riferiscono che anche altri paesi si stanno pentendo... C'è dell'altro.
Pfizer afferma a pagina 12 della monografia del prodotto che Paxlovid:
Ma non esiste un tale avvertimento per l'uso di nirmatrelvir/ritonavir da parte delle donne che allattano al seno.
Come ho sottolineato in precedenza in questo articolo, ogni dose di Paxlovid è composta da due compresse di nirmaltrelvir e una compressa di ritonavir.
Ciascun set di tre compresse deve essere assunto due volte al giorno per cinque giorni, iniziando entro cinque giorni dalla comparsa dei sintomi.
Ritonavir è stato utilizzato dal 1996 in persone che risultano positive al test per l'HIV.
È ben noto che causa condizioni gravi e pericolose per la vita tra cui: pancreatite, problemi del ritmo cardiaco, problemi al fegato, gravi eruzioni cutanee e reazioni allergiche.
Tuttavia, nirmatrelvir/ritonavir non è stato studiato nelle persone con insufficienza epatica.
E né Pfizer né le autorità governative consigliano di non assumere nirmatrelvir/ritonavir, ad esempio, alle persone con rischio di sviluppare una funzionalità epatica anormale (compresi coloro che hanno avuto epatite B, epatite C o risultati elevati dei test epatici).
Al contrario, stanno mettendo in prima linea gli anziani e coloro che vivono in povertà o comunque sono svantaggiati.
Un articolo della CBC News del 25 gennaio riporta che il vicedirettore della sanità pubblica canadese, Howard Njoo, raccomanda:
Il Quebec è uno dei primi posti preparati a iniziare a usarlo su queste persone vulnerabili.
Entro marzo sperano di ricevere abbastanza pillole per curare più di 25.000 persone.
Ciò include coloro che hanno,
Successivamente, apriranno la lista per gli altri.
Quindi sembra che i politici, i funzionari del governo e la Pfizer stiano alimentando la domanda usando lo stesso playbook che hanno fatto con i vaccini.
All'inizio stanno rendendo disponibile solo un numero relativamente piccolo di pillole. E i media tradizionali stanno aiutando a pubblicizzarlo.
Ad esempio, un singolo rapporto della CBC della giornalista di Montreal Verity Stevenson del 18 gennaio lo ha definito un farmaco "ambito" che è stato,
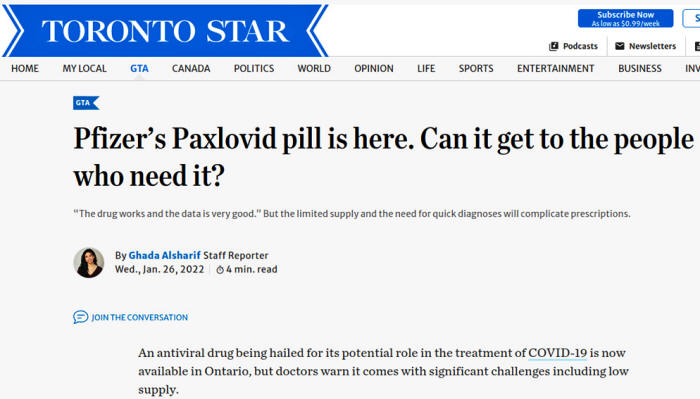
Ed ecco un altro esempio della copertura complessiva molto positiva; è nel Toronto Star di oggi.
Immagine della pagina del Toronto Star
Un articolo del National Post del 25 gennaio 2022 è in qualche modo un'eccezione:
Tuttavia, non menziona la maggior parte degli altri principali inconvenienti delle pillole.
Tuttavia, anche il governo federale canadese ammette, sul suo sito web per il grande pubblico sulla pillola:
E più in basso nella stessa pagina si dice che le persone dovrebbero segnalare qualsiasi effetto collaterale sospetto direttamente a Health Canada.
Sfortunatamente, tuttavia, sappiamo dai pochi rapporti, di gravi effetti e decessi causati, ad esempio, dalle iniezioni anti-Covid, che è altamente improbabile che tutti questi rapporti vengano conteggiati fedelmente e mostrati pubblicamente dai federali.
Da parte sua, la FDA ha chiesto a Pfizer di informarla su,
Ha inoltre stabilito che le strutture sanitarie e gli operatori sanitari che ricevono Paxlovid monitoreranno e segnaleranno gravi eventi avversi ed errori terapeutici.
Tuttavia, è altamente improbabile che ciò si traduca in un resoconto pubblico completo e onesto.
La FDA ha anche chiesto all'azienda di fornire ulteriori risultati degli studi relativi alla sicurezza e all'efficacia fino alla conclusione dello studio ad aprile.
Quindi non cercano nemmeno di fingere che si sia dimostrato sicuro ed efficace. Dopotutto, siamo nell'epoca farmacocenica della storia del nostro pianeta.
Ecco altre tre bandiere rosse tra le tante che circondano Paxlovid:
Queste cose non possono essere inventate.
Spero sinceramente che i dipendenti che, dietro le quinte, si oppongono alla pressione per immettere in molte persone Paxlovid, prevalgano.
|